1 引言(Introduction)
藥品及個人護理用品(PPCPs)是近年出現的一類新型環境污染物.研究表明, 傳統的污水處理工藝難以將PPCPs完全去除, 因此, 在污水處理廠出水、污泥及自然環境中能夠檢測出低濃度污染物(ng·L-1~μg·L-1)(Boyd et al., 2003;Jones et al., 2007).對乙酰氨基酚(AAP)是一種非甾體抗炎藥, 由于具有退熱鎮痛的效果而被廣泛使用(Neamut et al., 2013;Lin et al., 2013).AAP作為PPCPs中一種常被檢測出來的物質而受到廣泛關注(Feng et al., 2015).目前已有研究報道, AAP及其轉化產物在水環境存在潛在環境風險, 濃度為1.8 μg·L-1的AAP會對水生生物產生毒害作用(Sung et al., 2014;Kim et al., 2009).因此對AAP降解技術及規律的研究已然成為研究熱點.
近年來, 高級氧化技術(AOPs)在處理PPCPs方面應用非常多(Kim et al., 2009;Trovó et al., 2012).常用的AOPs主要包括芬頓氧化法、臭氧氧化法、UV/H2O2光化學氧化法等(Esplugas et al., 2007;張薛和趙璇, 2015).目前, 已有研究采用臭氧法、UV/TiO2、UV/H2O2等方法降解AAP, 并且都取得較好的效果.曹飛等通過臭氧氧化法有效地降解水中AAP, 同時對降解過程進行推測, 但發現臭氧氧化法對AAP的礦化程度較差;Su等利用響應面分析優化電芬頓法降解AAP的條件, 在反應40 min后, 實現AAP的去除率達到99%;Feng等在UV/H2O2體系中, 對低濃度AAP的降解機制進行研究, 同時分析了羥基自由基、各類陰離子及腐殖酸對中間產物的影響;Li等則重點研究了鹵化物對UV/H2O2降解AAP的影響.(曹飛等, 2014;Su et al., 2013;Feng et al., 2015;Li et al., 2015).UV/H2O2法不同于芬頓法和臭氧法, 因其不會產生二次污染而備受關注(Kim et al., 2009;Tan et al., 2014).目前, UV/H2O2降解AAP的研究更多的針對降解低濃度AAP、H2O2投量、存在的腐殖酸濃度及某些陰離子的研究, 而對于反應pH值、紫外功率和水中常見陰離子影響AAP降解過程的機制仍缺乏細致的研究.同時, 在先前采用UV/H2O2技術處理實際制藥生化尾水過程中, 在水中檢測到較高濃度的AAP, 因此本文進行UV/H2O2降解AAP的研究, 不僅考察H2O2投量、pH、紫外功率等對AAP降解效果的影響, 同時模擬實際廢水中存在大量HCO3-、NO3-的情況, 研究不同濃度下這兩種共存陰離子對AAP去除的影響, 以期為實際廢水的處理提供理論支撐.同時根據對反應中間產物的分析, 提出UV/H2O2降解AAP的可能途徑, 對優化AAP降解技術具有參考意義, 最后采用每一對數減少級電能輸入指標對UV/H2O2工藝的電能利用效率進行評價.
2 材料與方法(Materials and methods)2.1 實驗材料
實驗試劑:甲醇(色譜純, JT Baker);H2O2(質量分數=30%);N, O-雙(三甲基硅烷基)三氟乙酰胺(BSTFA, 99.0%, TCI);四氫呋喃(99.5%, TCI);AAP(98.0%, 國藥集團化學試劑有限公司)分子式為C8H9NO2, 結構式如圖 1所示.試驗中所用到的其他試劑皆為分析純或者優級純, 實驗用水為Milli-Q超純水儀所制的超純水.
圖 1

圖 1對乙酰氨基酚的結構式
2.2 試驗方法
根據對實際制藥園區生化尾水的分析, 檢測出一定濃度的AAP, 前期開展了AAP初始濃度分別為10.0、20.0、40.0及60.0 mg·L-1的降解效果實驗研究.為進一步研究AAP降解過程反應動力學及降解機理, 設定AAP初始濃度為40 mg·L-1.UV/H2O2試驗在一個有效體積為750 mL的圓柱玻璃反應器中進行, 分別由3種不同功率(5、10、15 W)的低壓紫外燈(λ=254 nm)提供光源.為保證反應均勻發生, 在反應器底部放置一個轉子, 反應器放置在磁力攪拌器上.內置紫外燈管的石英玻璃管套內放入反應器.用0.1 mol·L-1的NaOH和H2SO4調節溶液初始pH值, 向溶液中添加一定體積的H2O2溶液(質量分數=30%).反應開始后, 每隔5~10 min取樣, 測定AAP濃度、TOC及中間產物.本實驗通過對不同H2O2投量、溶液pH值、紫外功率及陰離子(HCO3-、NO3-)濃度的對照實驗, 考察UV/H2O2對AAP去除效果的影響.
2.3 分析方法2.3.1 AAP的測定方法
AAP濃度采用高效液相色譜(Agilent Technologies 1260 Infinity)進行測定(曹飛等, 2014), 利用外標法進行定量.色譜柱為Eclipse XDB-C18 (4.6 mm×150 mm;5 μm), 流動相為超純水和甲醇(V:V=70:30), 流速1.0 mL·min-1;柱溫30 ℃;紫外檢測器, 檢測波長為243 nm, 進樣量為20 μL.
2.3.2 中間產物分析方法
采用GC/MS對中間產物進行分析(Yang et al., 2008), 采用HP-5MS毛細管柱(30 m×0.25 mm×0.25 μm);GC設置條件:進樣口溫度280 ℃, 分流進樣20 μL;采用程序升溫, 初始溫度為60 ℃, 保持3 min, 以8 ℃·min-1的速率上升到280 ℃, 保持3 min;氦氣為載氣, 載氣流量為1.0 mL·min-1.MS設置條件:電離方式為電子轟擊源, EI源為70 eV;離子源溫度230 ℃.樣品進行GC/MS分析前需進行衍生預處理:取50 μL水樣于2 mL尖底氣相小瓶, 輕柔氮吹至水樣完全吹干后加入50 μL的色譜純四氫呋喃和20 μL的BSTFA, 加蓋密封置于簡易加熱器中40 ℃條件下衍生30 min, 而后進行GC/MS分析.
2.3.3 其他指標測定
采用島津TOC-VCPH分析儀測定TOC;pH由HANNA儀器有限公司HI-8424型pH計測定.水樣皆經過0.45 μm微孔濾膜過濾后進行分析測試.剩余H2O2濃度采用草酸鈦鉀分光光度法進行測定.
3 結果與討論(Results and discussion)3.1 不同實驗條件下AAP的UV/H2O2降解效果3.1.1 單獨UV、H2O2和UV/H2O2降解AAP
首先比較了采用單獨UV光照, 單獨H2O2氧化和UV/H2O2工藝分別降解40.0 mg·L-1AAP的效果.在UV功率為15 W, H2O2投量為250 mg·L-1時, 實驗結果見圖 2.
圖 2

圖 2 UV、H2O2和UV/H2O2對AAP降解效果的影響
由圖 2可知, 單獨H2O2氧化AAP時, AAP濃度基本保持不變.這表明H2O2很難破壞AAP分子中的化學鍵, 因此對其的降解幾乎為零;而在單獨UV光照過程中, 輻照20 min后, AAP濃度開始出現稍小程度的下降, 但去除率明顯不高, 低于7.0%.這說明雖然AAP在254 nm波長對紫外光有直接的吸收, 但這種吸收行為不易將AAP降解.而在UV/H2O2工藝中可以看出, AAP的濃度隨反應時間下降的趨勢非常明顯, 在反應60 min后, AAP的去除率達到95.52%, AAP的反應速率常數為0.0552 min-1, 氧化效果顯著.主要原因是紫外光激發H2O2產生具有強氧化性的羥基自由基(·OH), ·OH與有機物結合從而達到降解有機物的目的(馮欣欣等, 2015).主要反應過程見式(1)、(2).
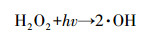
(1)

(2)
使用一級反應動力學公式擬合實驗數據, 得到R2=0.990, 因此AAP的降解符合擬一級反應動力學, 見式(3).
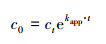
(3)
式中, c0為反應中AAP的初始濃度(mg·L-1);ct為反應中AAP隨時間變化的濃度(mg·L-1);t為反應時間(min);kapp為AAP的一級反應動力學常數(min-1).
3.1.2 不同H2O2投量對AAP降解效果的影響
對比紫外功率為15 W, pH為7.0, AAP初始濃度40 mg·L-1時, 不同H2O2投量(50、100、250、500、750 mg·L-1)對UV/H2O2降解AAP的影響, 實驗結果見圖 3.
圖 3

圖 3在UV/H2O2條件下H2O2投量對AAP去除效果的影響
從圖 3可知, 反應60 min后, H2O2投量從50增加到100 mg·L-1時, AAP去除率從56.3%增加到66.5%, AAP反應速率常數從0.01457增加到0.0188 min-1, 增幅較小;H2O2的投量從100增加到750 mg·L-1時, AAP的去除率都在顯著增加, 反應60 min后AAP的去除率由66.5%到100%, AAP反應速率常數從0.0188增加到0.10844 min-1.這說明AAP的去除率和降解速率常數均會隨著H2O2投量的增大而增加, 投量的增大對降解AAP降解具有明顯的促進作用.在Feng等的研究中也發現H2O2投量越大, AAP的去除效果越好, 同時反應時間也大幅度的縮短.分析其原因, 主要是由于在一定功率紫外輻照下, H2O2投量增加, 產生的·OH的數量也會增加, 從而提高反應速率, 提高AAP的去除率(Buxton et al., 1988).
有關研究表明, 過量的H2O2會抑制羥基自由基的氧化作用, 因為過量的H2O2對羥基自由基有一定程度的捕獲作用, 從而會使AAP反應速率常數降低(Wu et al., 2007).值得注意的是, 在本實驗中并未出現隨著H2O2投量的增加導致AAP降解速率常數的降低.分析原因, 可能是本實驗中H2O2的投量并未過量.
3.1.3 不同pH值對AAP降解的影響
在紫外功率為15 W, H2O2投量為250 mg·L-1, AAP初始濃度40 mg·L-1時, 考察不同的pH值(3.0、5.0、7.0、9.0、11.0)隨反應時間對UV/H2O2降解AAP的影響, 實驗結果見圖 4.
圖 4
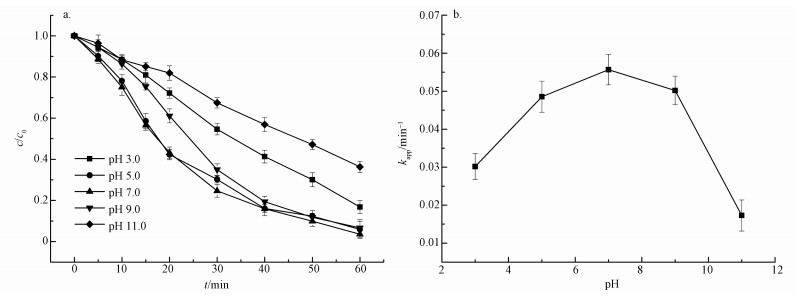
圖 4在UV/H2O2條件下pH值對AAP去除效果的影響
從圖 4可知, 不同的pH值下, 反應60 min后AAP的去除率呈現出隨著pH值的升高, 去除率增加后減小的趨勢, 在pH值為7.0時, 去除率最大.AAP去除率分別為83.22%、94.10%、96.44%、93.31%、63.71%.反應速率常數也呈現出相似的規律:pH為7.0時, 反應速率常數最大, 為0.05568 min-1;在pH由3.0升高至7.0時, 反應速率常數由0.03017增大至0.05568 min-1;而堿性條件下, pH值的繼續增大, 反應速率常數反而降低, 由0.05568降低至0.01729 min-1.說明在中性條件下, AAP降解效果最優, 酸性條件次之, 堿性條件不利于AAP的降解.在Tan等對比基于UV光照的高級氧化技術降解AAP的研究中也發現在中性條件下反應速率常數最大, 而當pH小于5.0或者大于9.0時, 反應速率常數都相對較低(Tan et al., 2014).該結果與本研究結果相似, 進一步說明pH對AAP降解過程產生了較大的影響.分析其原因主要是因為在pH 3.0時, UV/H2O2體系中更易形成HO2·而不是·OH, ·OH的形成受到限制勢必影響氧化效果, 在酸性范圍內增大pH值可以提高反應體系形成的·OH的數量, 因而反應速率會隨pH增大而增大;而在堿性條件下, 體系生成HO2-, HO2-作為一種·OH淬滅劑, 進一步與·OH反應生HO2·, 同時在pH大于9.0時, 水中的H2O2更易被分解為水和氧氣, 從而降低反應速率, 影響氧化效果(Christensen et al., 1982;Chu, 2001).
3.1.4 不同紫外功率對AAP降解的影響
探究在AAP初始濃度40 mg·L-1, H2O2投量為250 mg·L-1的情況下, 反應60 min的條件下, 不同的紫外功率(5、10、15 W)對UV/H2O2工藝降解AAP效果的影響, 實驗結果見圖 5.
圖 5
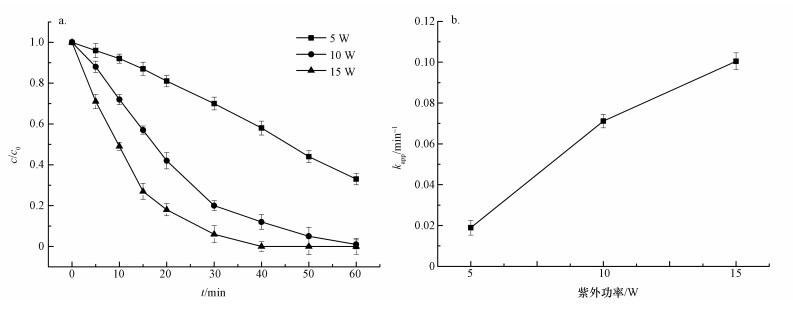
圖 5在UV/H2O2條件下紫外功率對AAP去除效果的影響
可以看出, 在不同的紫外功率下, 反應60 min后, AAP的去除率分別為66.74%、98.52%、100%, 去除效果均非常明顯.隨著紫外功率的增強, AAP的去除率逐漸增加, 反應速率常數也逐漸增加.當紫外功率從5增加到15 W時, AAP的反應速率常數從0.01893 min-1提高到0.10048 min-1, 這表明提高紫外功率對降解AAP反應具有相當明顯的促進作用.其主要原因是體系中H2O2投量一定時, 提高紫外功率能夠使H2O2更快地被分解而迅速的產生大量·OH, 提高反應速率, 縮短反應時間(汪力等, 2006).
3.1.5 HCO3-、NO3-濃度對AAP降解的影響
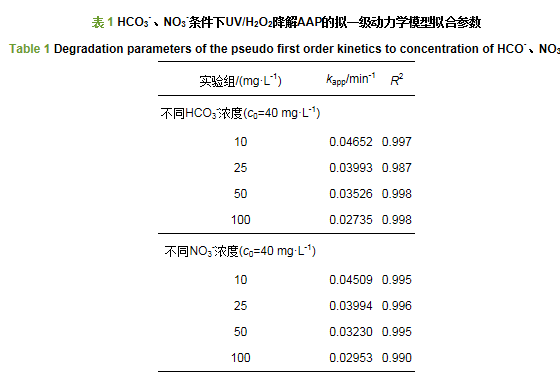
在紫外功率15 W, H2O2投量為250 mg·L-1的情況下(以磷酸鹽為緩沖液調節反應體系pH=7.0), 分別向水溶液中加入不同濃度的HCO3-和NO3-(10、25、50、100 mg·L-1)對比這兩種陰離子對UV/H2O2工藝降解AAP效果的影響, 實驗結果見圖 6和表 1.可以看出, 隨著HCO3-和NO3-濃度由10增加到100 mg·L-1時, 反應60 min后AAP的去除率均有小幅度的降低.HCO3-降解60 min后AAP的去除率由92.65%降到78.09%, 同時, AAP反應速率常數從0.04652增加到0.02735 min-1;NO3-降解60 min后AAP的去除率由91.50%降到81.82%, 同時, AAP反應速率常數從0.04509增加到0.02953 min-1.這說明HCO3-和NO3-濃度的增大均會抑制UV/H2O2工藝對AAP的降解作用.
圖 6
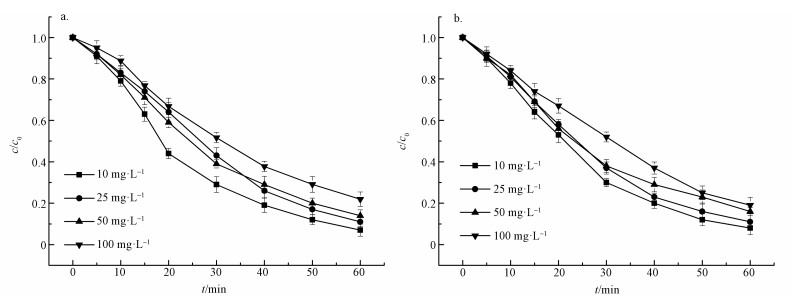
圖 6在UV/H2O2條件下HCO3-(a)、NO3-(b)濃度對AAP去除效果的影響
HCO3-作為一種羥基自由基的有效清除劑, 在通常情況下會與羥基自由基發生反應生成CO32-, 緊接著CO32-再與H2O2反應生成HO2·(李學艷等, 2013), 因此使得UV/H2O2工藝的反應速率常數降低.NO3-降低體系反應速率的原因主要在于一方面NO3-在紫外光的照射下就能產生·OH;另一方面由于NO3-對紫外光有較強的吸收, 從而起到惰性濾層作用, 阻止光線有效的穿過溶液(Du et al., 2007).而NO3-的吸收作用大于其產生·OH對AAP的氧化作用, 從而使得體系中產生·OH的效率下降, 因此抑制了UV/H2O2工藝對AAP的降解作用.
3.1.6 UV/H2O2對AAP的礦化作用
在pH 7.0, 紫外功率15 W, AAP濃度40 mg·L-1, H2O2投量為250 mg·L-1時, UV/H2O2體系, TOC去除率隨反應時間的變化情況如圖 7所示.由圖可以看出, TOC去除率幾乎呈直線上升趨勢, 在反應120 min后, TOC去除率達到39%.表明UV/H2O2對AAP的礦化效果顯著.
圖 7

圖 7 TOC去除率隨反應時間的變化
3.2 UV/H2O2降解AAP的主要降解產物及降解途徑分析
在pH 7.0, 紫外功率為15 W, H2O2濃度250 mg·L-1時降解AAP的主要產物主要如表 2所示.根據GC/MS對AAP降解中間產物的分析, 推測UV/H2O2氧化AAP的可能降解途徑如圖 8所示.AAP苯環上的乙酰基被·OH所取代, 生成乙酰胺(②)和對苯二酚, ·OH進一步將②氧化為乙醇酸(③), 再將③氧化成丙二酸, 最終被氧化成CO2和H2O (Yang et al., 2008).同時對苯二酚也被氧化生成對苯醌(④), ④的雙鍵被打開生成二羧酸, 最終被完全礦化(Andreozzi et al., 2003).AAP同時進行的降解過程還有AAP乙酰基上的被取代生成對氨基苯酚(⑥), 緊接著⑥上的氨基被氧化為NH4+, 從而生成苯酚(①), ①通過·OH取代作用也生成對苯二酚將進行上述降解途徑, 或者⑥生成對苯醌亞胺(⑤)而后進一步生成④, 同樣最終被完全礦化生成CO2和H2O(Liang et al., 2016).
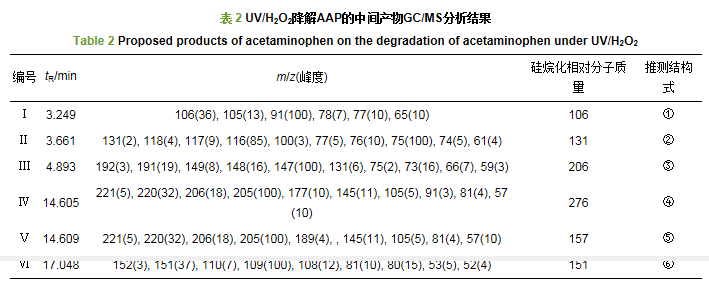
圖 8
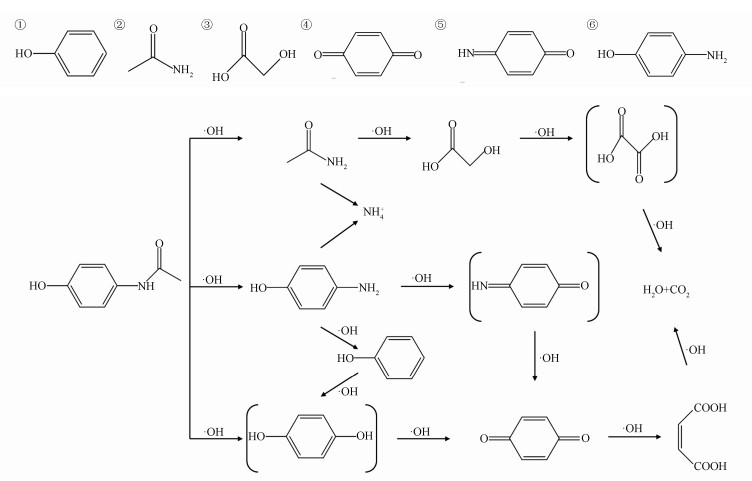
圖 8 UV/H2O2降解AAP的途徑推測
3.3 電能效率
在選擇水處理工藝時, 經濟成本是重點考慮因素之一.UV/H2O2過程會消耗電能, 而電能消耗又占據了運營成本中很大一部分.因此對水處理過程中的電能效率進行評價具有非常現實的意義.國際純粹與應用化學聯合會(IUPAC)針對高級氧化法(AOPs)在電能消耗方面提出采用電能效率評價指標(EEO)來評價水處理過程中的電能效率(Daneshvar et al., 1922).EEO表示在1 m3的污水中, 有機污染物濃度減少一個對數級所消耗的電能(Behnajady et al., 2009).電能效率計算公式見式(4)~(6)(Bolton et al., 2009).
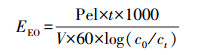
(4)
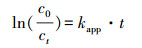
(5)
式中, Pel表示紫外燈輸出功率(kW);t表示輻照時間(min);V為反應水樣體積(m3);c0、ct分別表示有機污染物初始濃度和反應t時刻的濃度(mg·L-1);kapp為一級反應速率常數(min-1).
結合式(4)和式(5)可以得出更為簡便的計算公式(6).
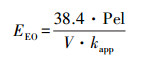
(6)
因此, 以紫外功率15 W, 水樣體積為0.00075 m3為例, 在H2O2投量250 mg·L-1, pH 7.0時, 反應速率常數為0.0552 min-1, 由式(6)可得, EEO為0.139 kW·h·m-3.這說明UV/H2O2的能耗較低, 經濟成本較低, 滿足實際工程應用的要求.
4 結論(Conclusions)
1) UV/H2O2降解AAP的反應符合偽一級動力學模型.同時在UV/H2O2體系中, 溶液pH、H2O2投量、紫外功率、兩種陰離子(HCO3-、NO3-)均對降解AAP產生影響, 尤其是加入這兩種陰離子會對反應體系產生抑制作用.
2) 通過對AAP降解過程中間產物分析, 初步判斷UV/H2O2過程中, 生成的·OH首先對苯環上的乙酰基進行取代, 生成苯酚類有機物, 然后中間產物進一步被氧化為醌類和結構更加簡單的有機物, 最終將有機物礦化為CO2和H2O.TOC分析表明UV/H2O2對AAP的礦化作用顯著.
3) UV/H2O2工藝的電能效率評價表明其能耗較低, 因此經濟成本較低, 在實際工程應用中, UV/H2O2降解AAP具有很大前景.(來源:環境科學學報 作者:茍璽瑩) |
